a) dove è ampiamente visibile
a) solo in forma gassosa
b) gassoso e raro
c) in tutti i paesi
d) a Zhodny Stan
1) cosa bisogna fare prima delle questioni fisiche? a) molecola b) punto di fusione c) chilometro d) oro2) che dire della sovraassicurazione e delle dimensioni fisiche?
a) secondo b) forza c) fusione d) sriblo
3) qual è la principale unità di massa nel sistema internazionale di unità?
a) chilogrammo b) newton c) watt d) joule
4) in quale momento un fisico considera vera l'affermazione?
a) dove è ampiamente visibile
d) in quanto ampiamente verificato sperimentalmente da varie fonti
5) in quale stato di discorso a parità di temperatura è maggiore la fluidità delle molecole?
a) per solido b) per raro c) per gassoso d) per tutti comunque
6) chi parla ha la fluidità di un ruggito inesorabile di molecole Cambia a causa delle temperature più basse?
a) solo in forma gassosa
b) gassoso e raro
c) in tutti i paesi
d) a Zhodny Stan
7) il corpo mantiene la sua forma originale. Quale stazione unitaria ha? il discorso che costituisce il corpo?
a) raro b) solido c) gassoso c) qualunque sia il caso
Aiuto per favore) cosa sai, mi piacerebbe fare)Parte A
UN. zattera
B. cabine sul fiume di betulla
Con. guidare
3. Modo – tse
UN. la fine della traiettoria
UN. υ = S
B. υ = S/t
Con. S = υt
D. t = S/v
UN. metro (m)
B. chilometro (km)
Con. centimetro (cm)
D. decimetro (dm)
UN. 1000 cm
B. 100 cm
Con. 10 cm
D. 100 dm
Parte B
1. La fluidità dello spackle è ancora di circa 20 m/s, quanto è in km/anno?
Parte C
3. Osserva il diagramma di flusso del corpo e fornisci feedback sull'alimentazione:
- perché l'elasticità del corpo è così antica?
-qual'è il percorso percorso dal corpo in 8 secondi;
1. Chiamatelo roc meccanico
UN. la posizione del corpo cambia nel tempo
B. cambiamento della posizione del corpo nel tempo dovuto all'uso di altri corpi
Con. il ruggito senza spina dorsale delle molecole da cui è formato il corpo
2. Quando una persona si trova su una zattera che galleggia sul fiume, questa crolla rapidamente
UN. zattera
B. cabine sul fiume di betulla
Con. guidare
3. Modo – tse
UN. la fine della traiettoria
B. una linea crolla come un corpo
Con. la distanza più breve tra il punto iniziale e quello finale del rukhu
4. Rukh è chiamato uguale perché
UN. per intervalli di tempo uguali il corpo deve percorrere gli stessi percorsi
B. a intervalli uguali di un'ora il corpo deve percorrere nuovi percorsi
Con. per qualsiasi intervallo di tempo il corpo deve percorrere gli stessi percorsi
5. Per calcolare la fluidità corporea media per un corpo irregolare, è necessario
UN. tutte le ore moltiplicano i roc per le strade di passaggio
B. diffondere il caos su tutta la strada per l'intera ora
Con. l'intero passaggio del percorso è suddiviso in tutta l'ora della rovina
6. La formula per trovare la fluidità di un flusso uniforme è simile alla seguente:
UN. υ=St
B. υ= S/t
Con. S = υt
D. t = S/v
7. L'unità principale del Sistema Internazionale è l'unità SI
UN. metro (m)
B. chilometro (km)
Con. centimetro (cm)
D. decimetro (dm)
8. In un metro (m) da localizzare
UN. 1000 cm
B. 100 cm
Con. 10 cm
D. 100 dm
Parte B
1. La fluidità dello stucco è di circa 20 m/s, quindi
UN. 20 km/anno
B. 36 km/anno
Con. 40 km/anno
D. 72 km/anno
2. Per 30 secondi il treno si è mosso uniformemente ad una velocità di 72 km/anno. Che percorso ha fatto il treno a quest'ora?
UN. 40 metri
B. 1 km
Con. 20 metri
D. 0,05 km
Parte C
1. Qual è la velocità media di uno struzzo, se prima corre 30 m in 2 s e fa un passo di 70 m in 0,05 s?
2. L'auto percorre parzialmente (30 km) da svedese medio 15 m/sec. Il vin della via Reshtu (40 km) è passato in 1 anno. Con che tipo di velocità media l'auto si schianta dappertutto?
Istruzioni dai robot Vikonannya.
45 dollari saranno spesi per lavori scientifici e fisici. Il lavoro è composto da 14 attività: 8 attività con una linea selezionata, 5 attività con una linea breve e 1 attività con una hot line.
Prima di selezionare un tipo di test, esistono 4 diversi tipi di test, di cui solo uno corretto. Al termine, cerchia il numero della riga selezionata. Se non hai cerchiato il numero, barra il numero cerchiato, quindi cerchia il numero del tipo corretto.
Per un'attività con una risposta breve, la risposta viene registrata nel lavoro designato per quella posizione. Se registri una riga errata, fissala e registrane una nuova.
La risposta al compito con la linea luminosa è registrata sull'arco adiacente. Durante i calcoli, è possibile utilizzare una calcolatrice non programmata.
Siamo lieti di ritirarci dall'ordine in cui viene data la puzza. Per risparmiare tempo, salta l'attività in modo da non terminarla immediatamente, quindi passa a quella successiva. Una volta finito tutto il tuo lavoro, perderai un'ora. Puoi voltarti prima di perdere le date.
Vengono assegnati uno o più punti per la corretta consistenza e piegabilità della pelle. Bali, sbarazzati di tutti i debiti per tutti i Vikonani, confonditi. Prova a vincere più premi e raccogliere più punti.
Applicare l'attività:
Dopo aver considerato la dovzhna della barra /, Sergiy, alunno di seconda media, ha scritto: = (14±0,5) div. Tse significa questo
1) barra dovzhina 13,5 cm o 14,5 cm
2) realizzare la lunghezza della barra da 13,5 cm a 14,5 cm
3) il prezzo per la sezione della linea è di 0,5 cm
4) la curvatura della linea è di 0,5 cm e la lunghezza della barra è di 14 cm
Può esserci una conferma indiretta del fatto del collasso disordinato delle molecole
A. Il fenomeno della dilatazione termica dei corpi.
B. Fenomeno di diffusione.
1) è vero solo L 3) l’insulto è vero
2) solo vero B 4) risentimento confermato errato
Una lepre che rimbalza può correre ad una velocità di 20 m/s. La volpe raggiunge i 2700 m in 3 settimane e il lupo può raggiungere una velocità di 54 km/anno. Scegli l'affermazione corretta sulla fluidità delle creature.
1) Una lepre può correre più veloce di una volpe o di un lupo.
2) La lepre corre più come una volpe, e talvolta più come un lupo.
3) La lepre corre più veloce del lupo, e anche più grande della volpe.
4) La lepre corre più veloce del lupo e della volpe.
Nel cortile ci sono diverse travi di legno con un volume di 0,18 m di pino, yalina, quercia e legno moderno. Lo spessore di queste specie legnose è presentato nella tabella. Il peso di qualsiasi legname è superiore a 100 kg. meno di 110 kg?
Acquista facilmente un libro elettronico in formato manuale, meravigliati e leggi:
Scarica il libro Lavoro diagnostico n. 1 da PHYSICS, 24 aprile 2013, grado 7, Opzione FI 7101 - fileskachat.com, scarica e scarica.
- Versione dei compiti chiave di fisica per la scuola primaria, classi 7-9, Gendenstein L.E., Kirik L.A., Gelfgat I.M., 2013
- Fisica, 7a elementare, Robot di controllo in un NUOVO formato, Godova I.V., 2013
- Progettazione per lavori di laboratorio in fisica, 7a elementare, Minkova R.D., Ivanova V.V., 2013
Accessori e libri:
- Fisica, 7a elementare, robot di verifica e controllo, Purisheva N.S., Lebedeva O.V., Vazheevska N.I., 2014
- Fisica, 11° grado, robot indipendenti, un libro di testo di base per organizzazioni educative (istituzioni di base ed educative), Gendenshtein L.E., Koshkina O.V., Orlov V.A., 2014
Al microscopio elettronico è possibile osservare e fotografare l'esterno di grandi molecole, ad esempio le molecole proteiche, che hanno un diametro di circa cm. Con l'aiuto della creazione di supermicroscopi (proiettori elettronici), è diventato possibile studiare le stesse molecole più piccole e grandi e di più attorno agli atomi. La possibilità di osservazione diretta di singole molecole e atomi è, in particolare, una prova iniziale e assolutamente inconfutabile della reale esistenza di queste particelle.
Riconsideriamo completamente l'evidenza indiretta che tutti i corpi fisici sono costituiti da molecole tenute insieme da interconnessioni e che non vi è alcun cambiamento nel flusso del gas, ad esempio nella sua elasticità. Ovviamente questo cambiamento è possibile solo grazie alla vicinanza reciproca delle molecole di stoccaggio del gas dovuta alla riduzione degli spazi tra loro.
La presenza delle forze di gravità e del movimento tra le molecole è chiaramente evidente nel potere dei solidi di preservarne la stabilità
modulo. Per deformazione lieve di un corpo solido è necessario segnalare un rumore significativo. Resta inteso che la tensione del corpo viene superata dalle forze di gravità e la pressione viene superata dalle forze di movimento tra le molecole.
Sarà necessario uno sforzo ancora maggiore per distruggere il corpo, ad esempio per farlo a pezzi. Ovviamente è necessario ridurre le forze di aggregazione tra le molecole, allontanando le molecole l'una dall'altra, in cui le forze di aggregazione diventano significativamente più piccole. L'impossibilità di spezzare il corpo semplicemente piegandone le parti dietro la superficie del male indica che le forze di consolidamento operano anche in piccole aree. A destra, le superfici del male appaiono sempre più o meno corte, e la dimensione della brevità supera significativamente la dimensione delle molecole (Fig. 68, a; le molecole sono rappresentate da punti). Pertanto, le parti del corpo (1 e 2) che sono collegate, quando più molecole si avvicinano alla superficie, sono sufficienti affinché si verifichino le forze di interazione.

È importante che la maggior parte delle molecole si trovino lontane le une dalle altre, in modo che tra loro non esistano forze di aggregazione. Se la superficie della sostanza è uniforme, quando sono collegate, più molecole si avvicineranno alla superficie delle forze adesive (Fig. 68 b), il che garantirà che non si verifichi l'“incollaggio” delle parti del corpo. È dimostrato che, ad esempio, due lastre di vetro accuratamente lucidate, applicate una dopo l'altra, aderiscono così male che è necessario un grande sforzo per separarle.
Ovviamente anche la saldatura, la brasatura e l'incollaggio di corpi solidi si basa sull'azione di forze adesive. Il metallo raro (o la colla) riempie l'intero spazio tra le superfici collegate. Pertanto, dopo che il metallo (colla) si è indurito, tutte le molecole nella zona di legame appaiono vicine l'una all'altra ad un livello sufficiente affinché le forze adesive possano operare.
Il flusso caotico ininterrotto delle molecole è più evidente nei fenomeni di diffusione e di flusso browniano.
Se metti una goccia di bromo sul fondo di un recipiente di vetro alto, il risultato sarà l'evaporazione attraverso una goccia di vino vicino al fondo
Infine si crea una palla di vapore che ha un colore marrone scuro. Questo vapore si espande rapidamente verso l'alto, mescolandosi con il vento, tanto che dopo un anno i gas nella nave raggiungono i 30 cm Ovviamente la miscelazione con il vapore del bromo è avvenuta non a causa dell'afflusso di gravità, ma nonostante tutto, nonostante la forza di gravità, i frammenti del bromo iniziale si dissolvono sotto la superficie e lo spessore del vapore è circa 4 volte maggiore per il bromo, sotto la superficie. In questo caso, la miscelazione potrebbe essere stata causata da un vortice caotico di molecole, nel quale processo le molecole di bromo venivano distribuite tra le molecole sulla superficie e le molecole venivano trasferite tra le molecole sul bromo. Osserva il fenomeno chiamato diffusione.
Nel 1827 Il botanico inglese Brown, esaminando rari preparati al microscopio, scoprì improvvisamente un simile fenomeno. Importanti nel paese, le minuscole particelle solide iniziarono a funzionare come roc senza palme, saltando da un posto all'altro. Come risultato di tali striature, le particelle descrivevano traiettorie a zigzag dalla forma più chimerica. Inoltre, questo fenomeno è stato scoperto più volte sia dallo stesso Brown che da altri ricercatori in diverse regioni e con diverse particelle solide. Più piccole erano le dimensioni delle particelle, più intenso era il fetore. Il fenomeno descritto era chiamato Brownian Rukh.

Il Brownie's Rukh può essere osservato, ad esempio, con una goccia d'acqua, una carcassa leggermente colorata o del latte, utilizzando un microscopio con un ingrandimento di cinquecento volte. Il diametro della parte browniana dovrebbe essere impostato sul diametro medio massimo consentito
Nella fig. 69 mostra un dipinto della traiettoria di uno dei pezzi dell'armatura. La rimozione di questa parte è stata effettuata attraverso 30 punti neri della pelle.
La ragione del rukhu browniano nelle caotiche molecole russe. È importante che la parte browniana abbia una dimensione minima (circa cento volte maggiore del diametro della molecola), possa muoversi facilmente sotto l'azione di impatti istantanei ma diretti di diverse molecole. Osservando la casualità delle molecole, i loro impatti sulla particella browniana sembrano essere in gran parte non compensati: da diversi lati, la particella viene colpita da una varietà di molecole, e anche la forza di impatto delle molecole vicine è del tutto la stessa. Pertanto, una parte di esso viene tolta da una parte o dall'altra e letteralmente lanciata su lati diversi nel campo visivo del microscopio. In questo modo, particelle browniane
Creano un collasso caotico delle molecole stesse, solo che le puzze collassano molto più delle molecole nella loro stessa grande massa.
L'increspatura browniana è una scala più ampia, ma con un ritmo più rapido di creazione del collasso termico delle molecole.
Il Browned Ruh è in grado di instillare nel GAZI, yaksho nel nomo Zvazhezhazhas, per finire gli altri hard -to -rhydki partins, lo yak del MAY MISTA, la ricalcità del nidificato ricaricabile, ispirato al genero del settore industriale.
Uno dei metodi per determinare la stasi permanente di Avogadro di Perrin, basato sulla guardia della rivoluzione browniana. Il valore è risultato pari a molecole per mole. Vimiruvannya preciso, vikonana usando un metodo diverso, ha dato per permanente Avogadro zagalnoy prendere valore immediatamente. È chiaro che una mole (talpa) si riferisce al volume della parola, la cui massa in grammi è simile alla massa molecolare dell'acqua. Più precisamente l'appuntamento va pregato all'appendice II. Il volume della parola 1000 volte maggiore di quello molare è chiamato kilomole (kmol).
Sulla base della teoria cinetica molecolare, è diventato possibile spiegare le molteplici potenze dei corpi e comprendere l'essenza fisica di una serie di fenomeni che si verificano in essi (conduttività termica, attrito interno, diffusione, cambiamento anch'io diventerò aggregato) . La teoria cinetica molecolare dei gas è chiaramente stagnante. Tuttavia, nel campo dei solidi, questa teoria ha permesso di stabilire alcune regolarità importanti. Tutta questa nutrizione verrà esaminata approfonditamente nelle sezioni successive delle altre parti del corso.
L’impianto a gas ideale è caratterizzato da tre parametri:
vice;
temperatura;
Ci nutriamo di ossessività (dolcezza).
1. Vice è una quantità scalare che caratterizza il rapporto di forza, normale al maidan, alla dimensione di questo maidan
 ;
;
 .
.
2. Temperatura è una quantità scalare che caratterizza l'intensità del movimento caotico delle molecole, che è proporzionale all'energia cinetica media di tale flusso.
 ,
,
 A
A  (2)
(2)
Scale di temperatura
Scala Celsius empirica ( T 0 C): 1 0 C =  0°C;
0°C;
Scala empirica Fahrenheit:  .
.
Culo: T
= 36,6 0 C;  .
.
Scala Kelvin assoluta: 
Pitomiy obsyag (spessore)
 pitomy obsyag – discorso tse obsyag in una massa di 1 kg;
pitomy obsyag – discorso tse obsyag in una massa di 1 kg;
 -spessore della massa del fiume con un volume di 1 m 3;
-spessore della massa del fiume con un volume di 1 m 3;  .
.
Teoria cinetica molecolare dei gas
1. Tutte le parole sono composte da atomi e molecole, che misurano circa 10 -10 m.
2. Gli atomi e le molecole del discorso sono separati da lacune distinte dal discorso. La conferma indiretta di questo fatto è un cambiamento nel volume corporeo.

3. Tra le molecole del corpo ci sono forze di reciproca attrazione e forze di reciproca attrazione allo stesso tempo.

La fluidità delle molecole è legata alla temperatura corporea: maggiore è la fluidità, maggiore è la temperatura. Pertanto, la fluidità delle molecole indica lo stato termico del corpo, la sua energia interna.
16. Principalmente legato alla teoria cinetica molecolare dei gas (teoria di Clausius). Rivalità al gas ideale (Mendeleev - Clapeyron) Rivalità di Clausius
 Possiamo contare la pressione che può essere riparata dalle molecole sul Maidan S.
Possiamo contare la pressione che può essere riparata dalle molecole sul Maidan S.
2a legge di Newton:





 . (1)
. (1)
Per una molecola:
Il numero di molecole in connessione con la base del parallelepipedo S quei riccioli v io T:
N=n io V= N io Sv io T (3)
n=N/ V – la concentrazione delle molecole, che è il rapporto tra il numero di molecole e lo spazio da esse occupato.
Per le molecole che trasmettono l'impulso al maidan S(in una delle tre linee rette reciprocamente perpendicolari, 1/3 delle molecole collassa, metà di esse, quindi 1/6 - sul maidan S)
 -fluidità quadrata media delle molecole
-fluidità quadrata media delle molecole


 , (4)
, (4)
 cinetica media. energia delle molecole in movimento
cinetica media. energia delle molecole in movimento
L'omaggio di Clausius:la pressione di un gas ideale è numericamente più avanzata 2/3 l'energia cinetica media delle molecole che arrivano al flusso di molecole in un unico rapporto.
Rivnyanya Mendelev - Clapeyron
La cerimonia lega i parametri del palcoscenico R , T , M , V .
 ,
,





 confronto Mendelev – Clapeyron (5)
confronto Mendelev – Clapeyron (5)
Prima legge di Avogadro: le kilomoli di tutti i gas per le menti normali occupano un nuovo compito, uguale 22,4 M 3 /kmol . ( Perché la temperatura del gas è più alta di prima T 0 = 273,15 K (0 °C) e il vice P 0 = 1 atm = 1.013 10 5 Pa, allora sembra che ci sia gas per menti normali .)

Equazione di Mendelev-Clapeyron per 1 mole di gas
 .
(6)
.
(6)
Rivnyanna Mendelev - Clapeyron per una massa di gas sufficiente
 numero di moli.
numero di moli.  ,
,




 (7)
(7)
Conclusioni private dell'equazione di Mendelev-Clapeyron
1
.

 mulino isotermico(Boyle – Legge di Marriott)
mulino isotermico(Boyle – Legge di Marriott)
2.


 Figura iconica(Legge di Gay-Lussac)
Figura iconica(Legge di Gay-Lussac)
3.


 campo isocornico(Legge di Charles)
campo isocornico(Legge di Charles)
17. Energia di un sistema termodinamico. La prima legge della termodinamica. Lavoro, calore, calore specifico, tutti i tipi
Energia– questo è il mondo della rovina della materia.
 .
.
Energia interna del sistema U l'antica somma di tutti i tipi di energie del movimento e delle interazioni delle particelle che formano l'intero sistema.
Robot esterno parametri di sistema
Calore– questo è un metodo di trasferimento di energia associato al cambiamento interno parametri di sistema
Cambiamenti tra calore e lavoro:
Il robot può trasformarsi senza alcuna restrizione su qualsiasi tipo di energia, la trasformazione del calore rientra nel quadro della 2° legge della termodinamica: si verifica solo un aumento dell'energia interna;
Il lavoro è associato a un cambiamento dei parametri esterni del sistema, il calore – con un cambiamento dei parametri interni.
Tutte e tre le quantità - energia, energia e calore - nel sistema CI sono misurate in joule (J).
L’impianto a gas ideale è caratterizzato da tre parametri:
vice;
temperatura;
Ci nutriamo di ossessività (dolcezza).
1. Vice è una quantità scalare che caratterizza il rapporto di forza, normale al maidan, alla dimensione di questo maidan
 ;
;
 .
.
2. Temperatura è una quantità scalare che caratterizza l'intensità del movimento caotico delle molecole, che è proporzionale all'energia cinetica media di tale flusso.
 ,
,
 A
A  (2)
(2)
Scale di temperatura
Scala Celsius empirica ( T 0 C): 1 0 C =  0°C;
0°C;
Scala empirica Fahrenheit:  .
.
Culo: T
= 36,6 0 C;  .
.
Scala Kelvin assoluta: 
Pitomiy obsyag (spessore)
 pitomy obsyag – discorso tse obsyag in una massa di 1 kg;
pitomy obsyag – discorso tse obsyag in una massa di 1 kg;
 -spessore della massa del fiume con un volume di 1 m 3;
-spessore della massa del fiume con un volume di 1 m 3;  .
.
Teoria cinetica molecolare dei gas
1. Tutte le parole sono composte da atomi e molecole, che misurano circa 10 -10 m.
2. Gli atomi e le molecole del discorso sono separati da lacune distinte dal discorso. La conferma indiretta di questo fatto è un cambiamento nel volume corporeo.

3. Tra le molecole del corpo ci sono forze di reciproca attrazione e forze di reciproca attrazione allo stesso tempo.

La fluidità delle molecole è legata alla temperatura corporea: maggiore è la fluidità, maggiore è la temperatura. Pertanto, la fluidità delle molecole indica lo stato termico del corpo, la sua energia interna.
16. Principalmente legato alla teoria cinetica molecolare dei gas (teoria di Clausius). Rivalità al gas ideale (Mendeleev - Clapeyron) Rivalità di Clausius
 Possiamo contare la pressione che può essere riparata dalle molecole sul Maidan S.
Possiamo contare la pressione che può essere riparata dalle molecole sul Maidan S.
2a legge di Newton:





 . (1)
. (1)
Per una molecola:
Il numero di molecole in connessione con la base del parallelepipedo S quei riccioli v io T:
N=n io V= N io Sv io T (3)
n=N/ V – la concentrazione delle molecole, che è il rapporto tra il numero di molecole e lo spazio da esse occupato.
Per le molecole che trasmettono l'impulso al maidan S(in una delle tre linee rette reciprocamente perpendicolari, 1/3 delle molecole collassa, metà di esse, quindi 1/6 - sul maidan S)
 -fluidità quadrata media delle molecole
-fluidità quadrata media delle molecole


 , (4)
, (4)
 cinetica media. energia delle molecole in movimento
cinetica media. energia delle molecole in movimento
L'omaggio di Clausius:la pressione di un gas ideale è numericamente più avanzata 2/3 l'energia cinetica media delle molecole che arrivano al flusso di molecole in un unico rapporto.
Rivnyanya Mendelev - Clapeyron
La cerimonia lega i parametri del palcoscenico R , T , M , V .
 ,
,





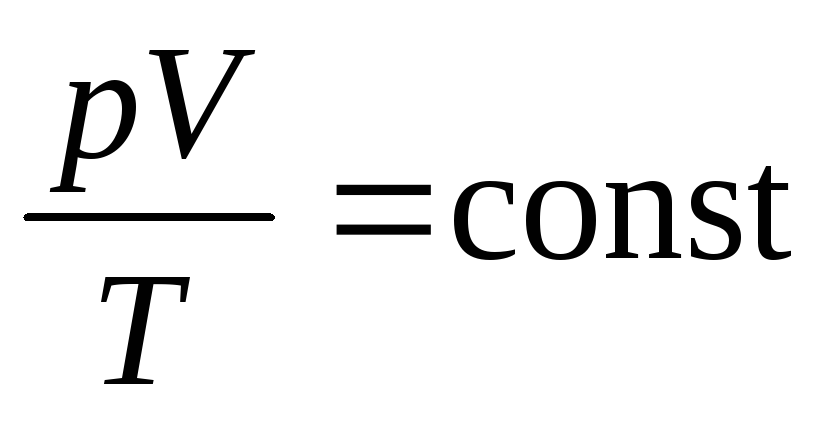 confronto Mendelev – Clapeyron (5)
confronto Mendelev – Clapeyron (5)
Prima legge di Avogadro: le kilomoli di tutti i gas per le menti normali occupano un nuovo compito, uguale 22,4 M 3 /kmol . ( Perché la temperatura del gas è più alta di prima T 0 = 273,15 K (0 °C) e il vice P 0 = 1 atm = 1.013 10 5 Pa, allora sembra che ci sia gas per menti normali .)

Equazione di Mendelev-Clapeyron per 1 mole di gas
 .
(6)
.
(6)
Rivnyanna Mendelev - Clapeyron per una massa di gas sufficiente
 numero di moli.
numero di moli.  ,
,




 (7)
(7)
Conclusioni private dell'equazione di Mendelev-Clapeyron
1
.

 mulino isotermico(Boyle – Legge di Marriott)
mulino isotermico(Boyle – Legge di Marriott)
2.


 Figura iconica(Legge di Gay-Lussac)
Figura iconica(Legge di Gay-Lussac)
3.


 campo isocornico(Legge di Charles)
campo isocornico(Legge di Charles)
17. Energia di un sistema termodinamico. La prima legge della termodinamica. Lavoro, calore, calore specifico, tutti i tipi
Energia– questo è il mondo della rovina della materia.
 .
.
Energia interna del sistema U l'antica somma di tutti i tipi di energie del movimento e delle interazioni delle particelle che formano l'intero sistema.
Robot esterno parametri di sistema
Calore– questo è un metodo di trasferimento di energia associato al cambiamento interno parametri di sistema
Cambiamenti tra calore e lavoro:
Il robot può trasformarsi senza alcuna restrizione su qualsiasi tipo di energia, la trasformazione del calore rientra nel quadro della 2° legge della termodinamica: si verifica solo un aumento dell'energia interna;
Il lavoro è associato a un cambiamento dei parametri esterni del sistema, il calore – con un cambiamento dei parametri interni.
Tutte e tre le quantità - energia, energia e calore - nel sistema CI sono misurate in joule (J).





